C'est le 2 août 1939 qu'Albert Einstein publie une lettre au Président Roosevelt pour le prévenir du risque de voir apparaître une bombe atomique après la découverte de la réaction en chaîne. Six ans plus tard, quasiment jour pour jour, la bombe atomique tombe sur Hiroshima. Pourquoi je vous parle de ça ? Parce qu'aujourd'hui, une nouvelle technologie fait son apparition en biologie moléculaire. Elle est tout aussi fascinante qu'effarante, car elle permet de modifier génétiquement toute la population d'une espèce en quelques générations. Et ironie du sort, cette technologie s'appelle MCR : « Mutagenic Chain Reaction ».
Le principe
Nous et d'autres espèces sexuées sommes diploïdes. C'est-à-dire que nous possédons chacun de nos gènes en deux exemplaires. Une version (allèle) provient de la mère et l'autre provient du père. Lors de la formation des gamètes, le mécanisme de méiose choisit aléatoirement une version de ce gène pour fabriquer un spermatozoïde ou un ovocyte. Ainsi, lors de la fécondation, chaque allèle a une chance sur deux de se transmettre à la descendance.
La technologie de « forçage génétique » ou « gene drive » biaise ce mécanisme de l'hérédité en rendant le gène souhaité héritable à presque 100 %. En quelques générations seulement, un trait génétique peut alors se répandre dans toute la population.
Comment ça fonctionne ? Je vous le donne en mille. Encore un coup de ce CRISPR-Cas9...
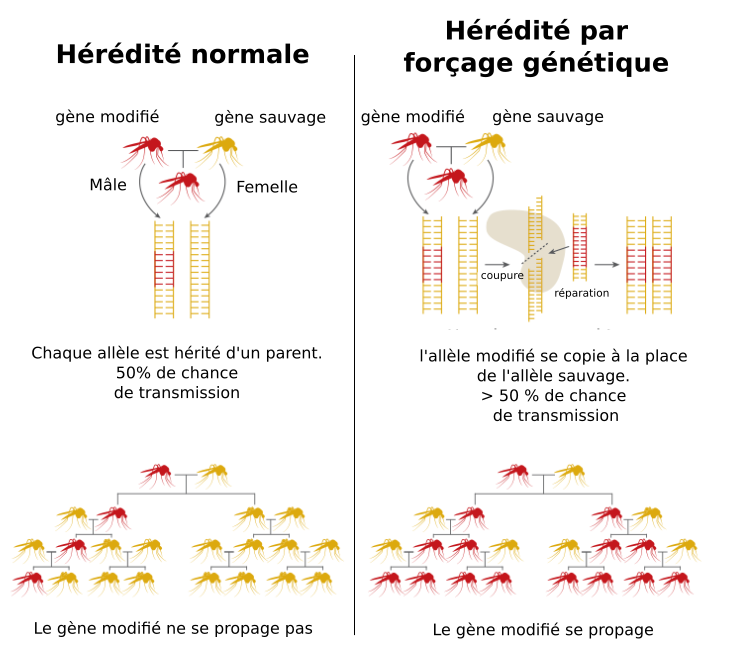
source de l'image
Un gène vraiment égoïste
L'idée est de créer un gène artificiel de sorte qu'il puisse détruire son allèle homologue sauvage et s'y copier à la place. Pour cela, on associe au gène d'intérêt une séquence codant pour l'endonucléase Cas9 ainsi que l'ARN guide qui cible le même gène à l'état sauvage grâce à des séquences homologues (H1, et H2 sur le schéma). Cet ensemble s'apelle une « cassette ». Si dans une cellule, l'allèle sauvage se trouve avec cette cassette, il est localisé et découpé par le complexe Cas9-ARN guide. Le trou béant qui en résulte est corrigé en prenant comme modèle la séquence homologue de l'allèle disparu qui n'est autre que la séquence de la cassette. On passe d'un état hétérozygote à une cassette à un état homozygote à deux cassettes. Lors de la fécondation, la probabilité de transférer ce nouveau gène passe ainsi de 50 % à 100 %.
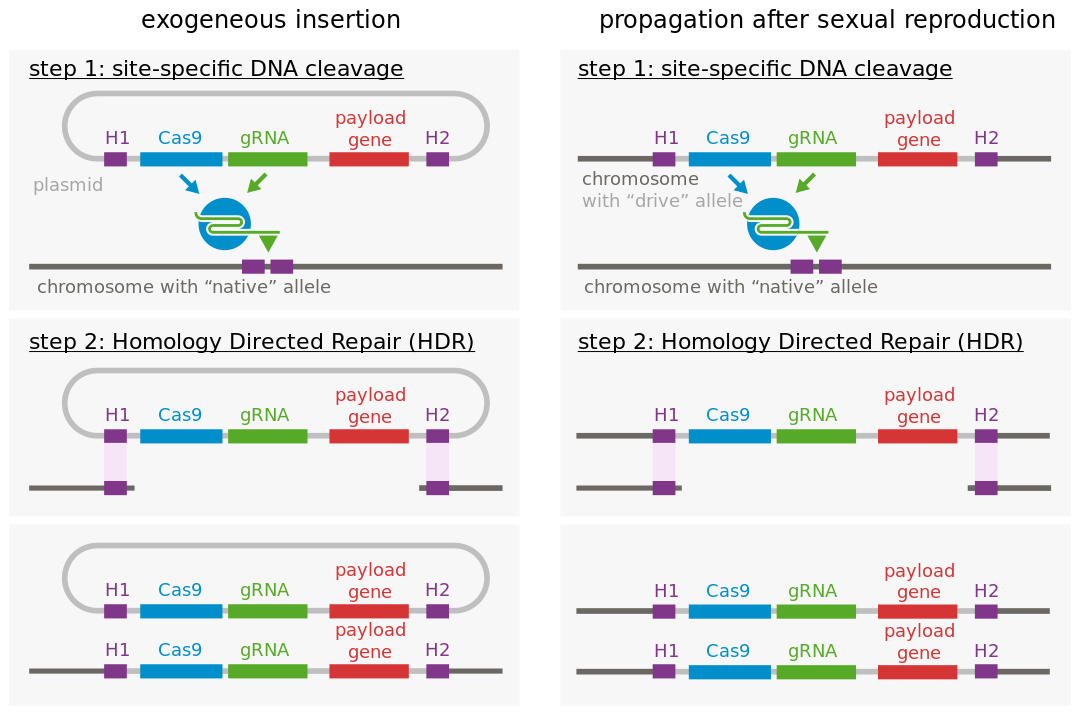
H1, H2 : site de reconnaissance de l'ARN guide. Payload gene : gène que l'on désire voir se propager. gRNA : ARN guide. Cas9 : endonucléase
source de l'image
Un moyen de lutte contre le paludisme
Une des premières applications de cette technologie serait de lutter contre la propagation du paludisme par les moustiques. Il suffirait d'introduire quelques moustiques disposant d'un gène les empêchant de transmettre le parasite. En quelques générations, ce nouveau trait génétique se répandrait dans toute la population. Et cela même si le gène n'apporte aucun avantage au moustique, voire même, si dans une moindre mesure, il est délétère. Il s'agit d'un face à face entre l'ingéniosité humaine et la sélection naturelle.
Le danger ?
Les applications de la technologie gene drive sont infinies et nombreux sont ceux qui vont vouloir jouer avec, que ce soit pour lutter contre des maladies ou pour l'amélioration de l'exploitation agricole. Et pourquoi pas plus tard, pour améliorer l'homme en le rendant plus fort et en meilleure santé ?
Derrière ces belles promesses, il y aura, je pense, inévitablement des effets de bord et toutes les précautions devront être prises. Qu'adviendrait-il par exemple si un mauvais gène était introduit lors d'un gene drive chez l'homme? Et si le gène passait d'une espèce à l'autre ? Quelles seraient les répercussions sur l'écosystème ? Que se passerait-il si une mutation apparaissait dans une cassette avec un effet non escompté ?
Bref, une technologie à mon sens imprédictible, dont le moratoire mondial a été rejeté lors de la réunion de la biodiversité de l'Organisation des Nations Unies en décembre 2016.
Références
- The creation and selection of mutations resistant to a gene drive over multiple generations in the malaria mosquito
- Site-specific selfish genes as tools for the control and genetic engineering of natural populations
- Faut-il relâcher le « gene drive » dans la nature ?
- Modeling the Manipulation of Natural Populations by the Mutagenic Chain Reaction
Remerciements
Ce site est versionné sur GitHub. Vous pouvez corriger des erreurs en vous rendant à cette adresse
Go Top