C'était la news de la semaine dernière. La première thérapie génique appelée Kymriah™ a été autorisée aux États-Unis par la FDA dans le traitement d'un cancer, en l'occurrence la leucémie aiguë lymphoblastique.
Ce traitement est une immunothérapie et va plus loin que l'immunothérapie classique à base d'anticorps anti-CTLA4/anti-PD1 (voir la vidéo sur le cancer de @scienceEtonnante, il en parle dans sa conclusion).
Elle repose sur ce qu'on appelle un « transfert adoptif de cellules »:
- on prend les cellules immunitaires du patient (lymphocyte T);
- on les modifie génétiquement pour qu'ils ciblent les cellules cancéreuses;
- puis on les réinjecte au patient;
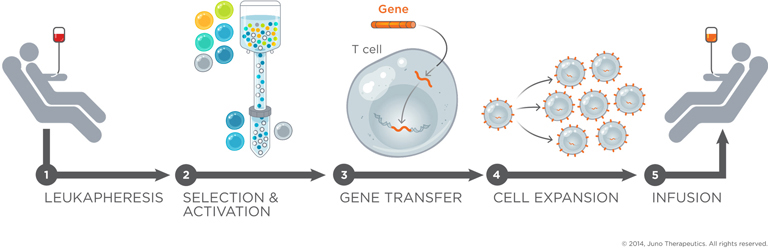
Génial non ? Alors, voyons de plus près comment fonctionne cette thérapie étape par étape.
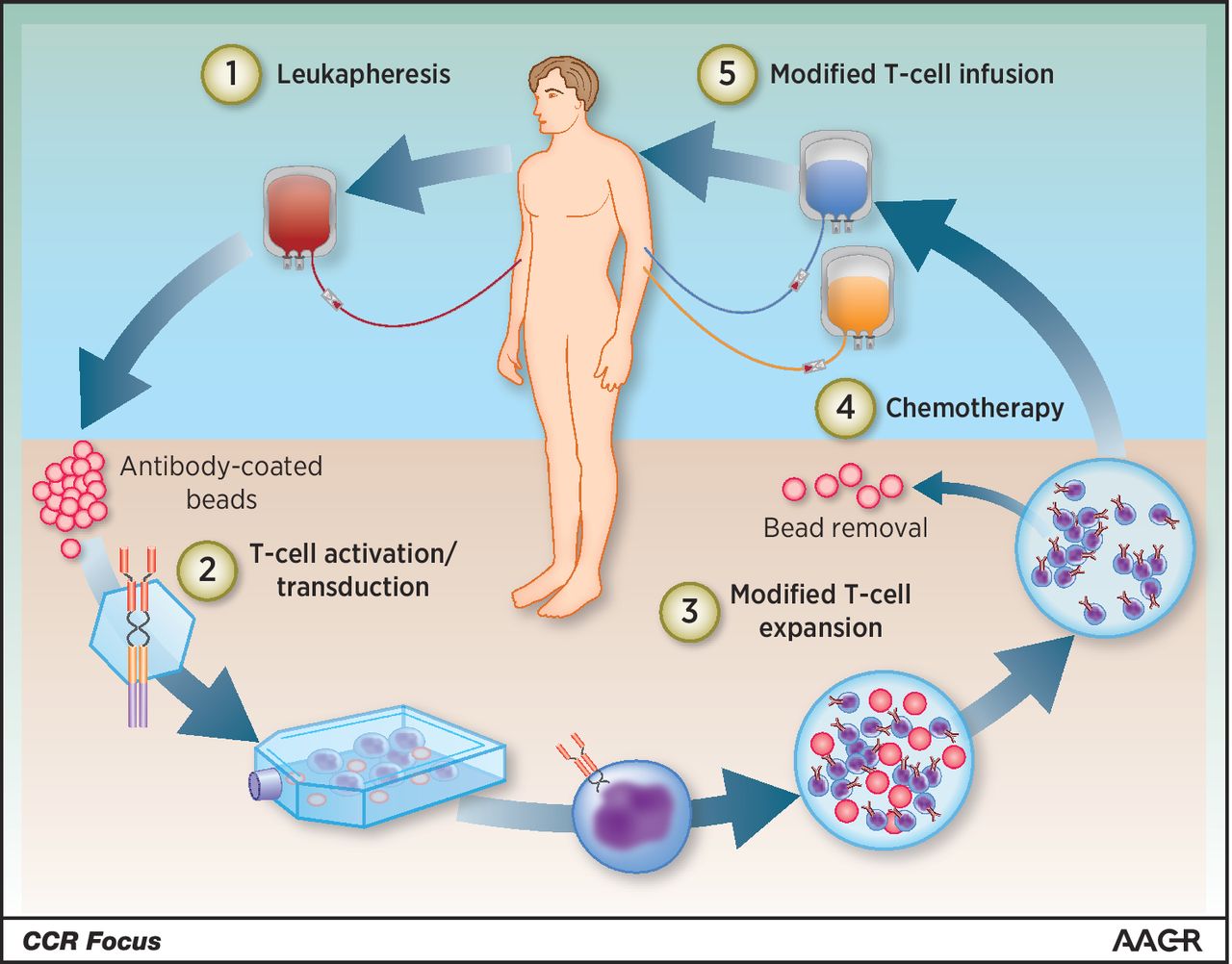
source de l'image
Étape 1 : Leucophérèse et récupération des lymphocytes T
La première étape consiste à extraire du sang, les lymphocytes T.
On réalise pour cela une leucophérèse. C'est un peu comme une prise de sang, sauf qu'ici tous les globules blancs (leucocytes) sont filtrés et le reste (globule rouge, plaquettes ...) retourne directement dans la circulation sanguine.
De ces leucocytes, on récupère les lymphocytes T en utilisant différentes techniques de séparation comme la centrifugation ou encore des billes magnétiques couplées à des anticorps spécifiques.
Étape 2 : Culture cellulaire
À partir de là, on a besoin de mettre les cellules en culture pour qu'elles se divisent. Un prérequis pour la transfection virale qui fera suite.
À l'état normal, les cellules T se divisent après activation par des cellules présentatrices d'antigènes ou dendrocytes (voir les supers vidéos de @unPeuPointu). On pourrait en ajouter, mais le risque c'est qu'au moment de la réinjection au patient, ces cellules étrangères déclenchent un rejet immunitaire. On préfère alors utiliser des billes magnétiques recouvertes d'anticorps qui se font passer pour des dendrocytes artificielles. Après l'activation, il suffira de les enlever avec un aimant.
Étape 3 : Transfection virale et récepteurs chimériques
C'est maintenant que la manipulation génétique commence. Un virus ARN utilisé comme vecteur, va venir intégrer un gène dans le génome du lymphocyte T pour qu'il exprime à sa surface un récepteur chimérique appelé CAR (Chimeric antigen recepteur) capable de reconnaitre les cellules tumorales. C'est le même mécanisme qu'avec n'importe quel virus ARN comme le VIH.
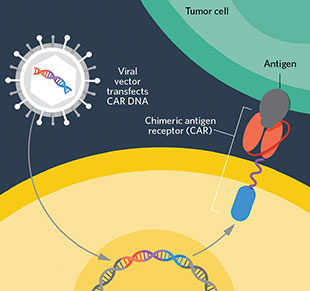
source de l'image
Les CAR ou CAR-T sont dits chimériques, car ils sont constitués artificiellement d'un domaine extramembranaire similaire à la portion variable des anticorps. Et d'une partie intracytoplasmique similaire aux récepteurs des cellules T permettant de déclencher le signal d'activation du lymphocyte (un motif ITAM pour les connaisseurs).
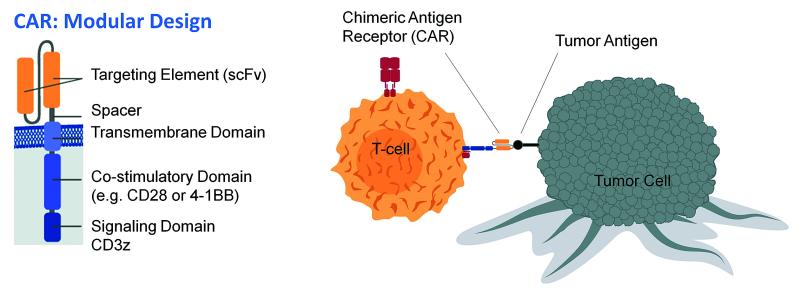
source de l'image
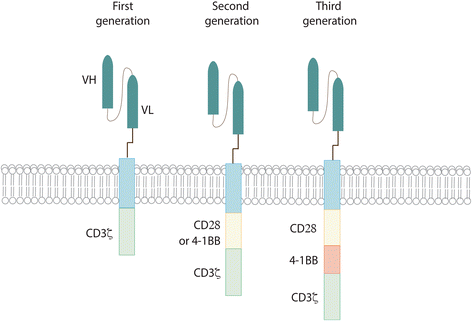
source de l'image
Dans le cas du Kymriah™, les CAR-T sont conçus pour qu'ils reconnaissent spécifiquement les antigènes CD-19 présents à la surface des cellules cancéreuses (mais aussi des lymphocytes B normaux). Lorsque ces nouveaux lymphocytes T génétiquement modifiés seront en contact avec les cellules cancéreuses, ils s'activeront et entraîneront une réponse immunitaire ciblée.
Étape 4 : Préparation du produit
Il ne reste plus qu'à préparer nos cellules pour l'injection. Les billes magnétiques sont retirées. Les microbes éliminés en utilisant des rayons UV. Etape critique, car on s'apprête à réinjecter un produit dans la circulation du patient.
Étape 5 : Adminstration au patient
Les lymphocytes T génétiquement modifiés sont administrés au patient. En général, le patient est préparé à recevoir le traitement avec une chimiothérapie lympho-déplétive. L'activation des cellules T est aussi soutenue par l'administration d'interleukine-2, une molécule stimulant les lymphocytes T.
Quant aux effets indésirables, ils existent. Le relargage excessif des cytokines par les lymphocytes T activés est responsable du syndrome de relargage des cytokines. Et n'oublions pas que ces CAR-T anti-CD19 ciblent également les lymphocytes B avec le risque d'un déficit de l'immunité.
Et l'efficacité du traitement ?
D'après cette étude, l'efficacité des CAR-T anti-CD19 est vraiment bonne avec 90% de rémission complète dans la leucémie lymphoïde aiguë.
D'autres chercheurs ont déjà essayé la thérapie cellulaire adoptive sur d'autres cancers, notamment les cancers solides. Des résultats concluants ont déjà été obtenus dans le mélanome métastatique. Dans ce cas, les lymphocytes expriment un récepteur reconnaissant des antigènes spécifiques du mélanome (MART-1).
Malheureusement la complexité technique de ces thérapies personnalisées rend inaccessible le traitement. Le Kymriah™ couterait environ 475 000 dollars!!! Avec ce nouveau traitement sur le marché, il y a de quoi creuser les inégalités dans la santé... surtout aux États-Unis.
Reference
- Principes de la thérapie cellulaire par transfert adoptif à base de Tumor Infiltrating Lymphocytes
- CAR T Cells: Engineering Patients’ Immune Cells to Treat Their Cancers
- Current approaches to increase CAR T cell potency in solid tumors: targeting the tumor microenvironment
- Safe engineering of CAR T cells for adoptive cell therapy of cancer using long‐term episomal gene transfer
- Chimeric antigen receptor T cells: a novel therapy for solid tumors
Merci aux relecteurs
@Jnsll
@HervePerdry
Ce site est versionné sur GitHub. Vous pouvez corriger des erreurs en vous rendant à cette adresse
Go Top